Analysestrategie bei der Aufklärung von Intoxikationsverdachtsfällen: Man findet nur das, was man sucht
DOI: https://doi.org/10.47184/td.2024.03.07Eine gründliche Fallrecherche sowie die Zusammenschau von Symptomatik und klinisch-chemischen Parametern bilden bei der Aufklärung von Intoxikationsverdachtsfällen die Basis für die Auswahl der optimalen, individuellen Analysestrategie und haben einen entscheidenden Einfluss auf die Bearbeitungsdauer und Aussagekraft der Untersuchungen. Das breite Spektrum an toxisch wirksamen Substanzen bedarf verschiedener Analysesysteme und der Kenntnis der analytischen Grenzen zu deren Nachweis. Vor allem toxikologische Screenings erfordern Erfahrung in der Beurteilung und sind oft der geschwindigkeitsbestimmende Schritt zwischen Anforderung und Befundung. Je nach Fragestellung können immunchemische oder sensitivere und spezifischere chromatographische Messverfahren eingesetzt werden.
Schlüsselwörter: Analysestrategie, Toxidrome, Intoxikation, Screening, Konzentrationsabschätzung
Der Nachweis toxisch wirksamer Substanzen kann in verschiedenen Szenarien wichtig sein. Neben akzidentiellen Intoxikationen oder Überdosierungen im Rahmen des Konsums von Missbrauchssubstanzen kommen zum Beispiel auch Suizidversuche oder die Beibringung durch Dritte vor. Das Substanzspektrum reicht von sehr kleinen Molekülen wie Methanol, Ethanol und Propanol bis hin zu größeren Molekülen wie etwa bestimmten Pflanzentoxinen. Dieses sehr heterogene Feld kann nicht umfassend durch ein einzelnes Analysesystem abgedeckt werden.
Besonders zeitkritisch ist die Aufklärung, wenn aus dem Ergebnis eine direkte therapeutische Konsequenz folgt. Bei einer gezielten Fragestellung für bestimmte Substanzen kann dies – in Abhängigkeit der Ausprägung der Symptomatik der Betroffenen – bereits bei der Anforderung entschieden werden. Hier sind Substanzen am wichtigsten, die eine Antidot-Therapie erfordern. Darüber hinaus bedingen einige Intoxikationen wie mit Trizyklischen Antidepressiva (TCA) aufgrund einer starken Wirkung auf kritische Organsysteme eine engmaschige, intensive Überwachung („intermediate care“; IMC).
In den Fällen, in denen keine gezielte Fragestellung vorliegt, wird die Dringlichkeit oft anhand der Symptomatik festgelegt. Prinzipiell werden toxikologische Analysen nicht nur bei konkretem Verdacht, sondern auch zum Ausschluss einer Intoxikation angefordert. Aufgrund dieser Punkte besteht – in unterschiedlicher Ausprägung – die Notwendigkeit einer möglichst raschen Diagnostik. Im Optimalfall hat man zu jeder Zeit (24/7) Zugang zu einer solchen Analytik.
Um möglichst zügig ein Ergebnis liefern zu können, spielt die initiale Auswahl des erfolgversprechendsten Analysesystems eine zentrale Rolle. Oft sind hier Informationen über die Auffindesituation, die Symptomatik sowie über klinisch-chemische Parameter der Betroffenen entscheidend. Nach Auswahl des Analysesystems wird über eine möglichst breite, ungerichtete („general unknown“) oder gerichtete („multi target“) Analyse (Screening) – meist im Serum, aber gegebenenfalls auch im Urin – versucht, relevante Substanzen zu identifizieren. Bei Urin ist zu beachten, dass substanzabhängig Metabolite miterfasst werden und dass gegebenenfalls Phase-2-Metaboliten wie zum Beispiel Glucuronide gespalten werden müssen. Danach erfolgt eine Konzentrationsabschätzung im Serum zur Einschätzung einer potenziell toxischen Wirkung. Abhängig von der Potenz der Wirkstoffe, die sich in zu erwartenden Konzentrationsbereichen widerspiegelt, müssen die Analysemethoden eine große Konzentrationsbreite abdecken. Anschließend muss die ermittelte Konzentration toxikologisch eingeordnet werden, um eine potenziell toxische Wirkung in direkter Kommunikation mit dem behandelnden ärztlichen Personal anzunehmen oder auch auszuschließen (Abb. 1).
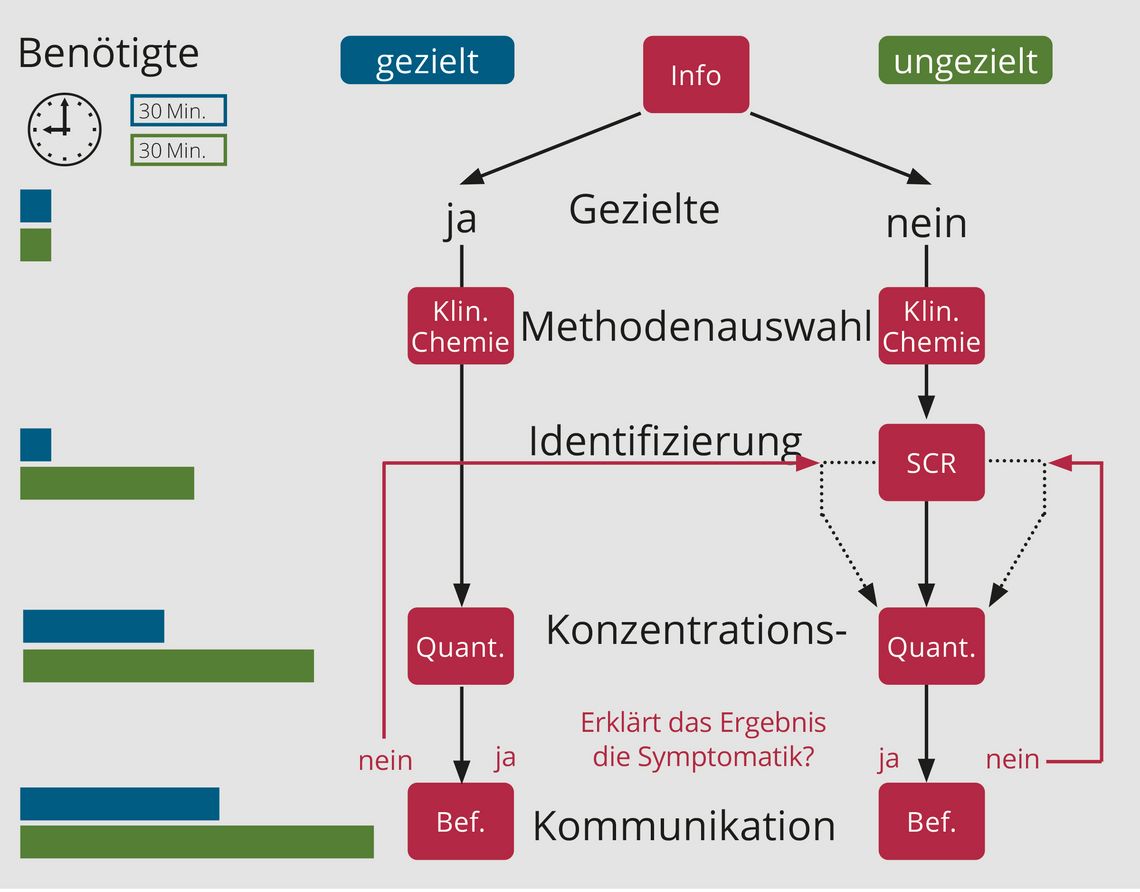
Abb. 1: Ablauf einer ungezielten/gezielten toxikologischen Analyse von der initialen Fallrecherche (Info) über mögliche klinisch-chemische Analysen zur Auswahl der erfolgversprechendsten Analysemethode, gefolgt vom Schritt der Identifizierung mittels Screening-Methode (SCR) sowie von der Konzentrationsabschätzung (Quant.) bis hin zur Einordnung der Konzentration und der Kommunikation mit dem behandelnden ärztlichen Personal (Bef.).
Auswahl der Analysestrategie
Die Fragestellung ist entscheidend für den Ablauf in der Bearbeitung und der davon abhängigen Zeit, bis ein zielführendes Ergebnis vorliegt. Lassen die Auffindesituation oder andere Informationen eine Einschränkung des Substanzspektrums bzw. die Begrenzung auf eine oder mehrere Substanzen zu, lässt sich die Analytik sehr beschleunigen: Das in der Regel recht zeitaufwendige Screening entfällt. Außerdem kann man bei einer konkreten Fragestellung oft auch eine bestimmte Substanz sicher ausschließen. Eine weitere, sehr zentrale Frage zu Beginn des Bearbeitungsprozesses ist die Auswahl des optimalen Nachweisverfahrens. Bereits hier können Informationen des Notarztes bzw. des Rettungsdienstes wertvolle Informationen liefern. In bestimmten Fällen werden beispielsweise im Rahmen der Erstversorgung Antidota eingesetzt, die eine durch bestimmte Wirkstoffe verursachte Symptomatik sehr rasch verbessern können. Tritt zeitnah nach Gabe eines Antidots eine Verbesserung ein, so ist dies ein Hinweis auf die Präsenz einer Substanz dieser Substanzklasse. Bei Intoxikationen mit Opioiden bzw. Benzodiazepinen kann es beispielsweise unter der Gabe des Antidots Naloxon bzw. Flumazenil zu einem raschen Aufklaren kommen. Die analytische Strategie sollte in diesem Fall in diese Richtung fokussiert werden.
Daneben kann auch die Symptomatik der Betroffenen wertvolle Hinweise auf wirksame Substanzen liefern (Toxidrome: Opioid-Syndrom, Anticholinerges Syndrom u. a.). Besonders aussagekräftig sind zentrale Körperfunktionen wie Atmung, Blutdruck, Herzaktivität, Körpertemperatur, Transpirationsaktivität sowie Bewusstseinslage und Pupillenweite. Zusätzlich können in der Regel zeitnah verfügbare klinisch-chemische Parameter wie etwa Elektrolyte, pH-Wert oder Osmolalität sowie daraus berechenbare Größen wie osmotische Lücke oder Anionenlücke erkenntnisreich sein. Sind etwa diese berechneten Größen erhöht, kann das auf entsprechend aktive Substanzen wie Methanol oder Ethylenglykol hinweisen – was einen zeitnahen Einsatz eines Antidots erfordert. Diese recht kleinen Moleküle sowie deren teils toxische Metabolite können häufig nicht in klassischen Wirkstoff-Screenings, sondern in der Regel nur mittels gaschromatographischen Analysen erfasst werden.
Vor allem bei entsprechender Symptomatik kann es sinnvoll sein, schnell verfügbare immunchemische Tests einzusetzen. Im Fall einer Aufnahme/Überdosierung von Herzglykosiden können die kardiale Funktionalität und gegebenenfalls klinisch-chemische Parameter, zum Beispiel Elektrolyte, auffällig sein. Durch die immunchemische Bestimmung von Digoxin oder Digitoxin können aufgrund von Kreuzreaktivitäten auch strukturverwandte Moleküle aus der Klasse der Herzglykoside bei entsprechend hoher Konzentration nachgewiesen werden. Darüber hinaus können Immunoassays für häufig eingesetzte Substanzen wie Paracetamol und Salicylate bei entsprechender Symptomatik oder Verdacht zielgerichtet eingesetzt werden, um möglichst schnell eine effektive Therapie zu ermöglichen.
Substanzidentifizierung
Kann aufgrund der Auffindesituation die Fragestellung auf eine oder mehrere Substanzen beschränkt werden, so kann auf ein Screening verzichtet und direkt eine Konzentrationsabschätzung – in der Regel unter Nutzung isotopenmarkierter Standards – durchgeführt werden, wenn die vermuteten Substanzen die Symptomatik erklären würden. Ist keine Einschränkung der potenziell ursächlichen Wirkstoffe möglich oder erklären die im Zuge einer gezielten Analyse nachgewiesenen Wirkstoffe die vorliegende Symptomatik nicht, führt man häufig ein möglichst breites Screening mittels Flüssigchromatographie-Massenspektrometrie (LC-MS) oder GC-MS durch.
Die Nachweisbarkeit einer Substanz hängt wesentlich von deren Struktur ab. Massenspektrometrische Verfahren sind hier besonders geeignet, da detaillierte strukturelle Informationen des Moleküls erfasst werden können. Dabei werden meist Scan-Messmodi für „untargeted“ oder Multitarget-Analysen genutzt. Nach der Ionisation der Moleküle erfolgt deren Fragmentierung. Die so generierten, substanzspezifischen Fragmentspektren aus der Probe werden letztendlich mit einer Bibliothek abgeglichen. Anschließend wird eine Hitliste erstellt. Diese muss mit analytischer Erfahrung individuell bewertet werden, um letzten Endes eine Substanz sicher zu identifizieren bzw. in einer näheren Auswahl weiter zu berücksichtigen (SCR B; siehe Abb. 2).
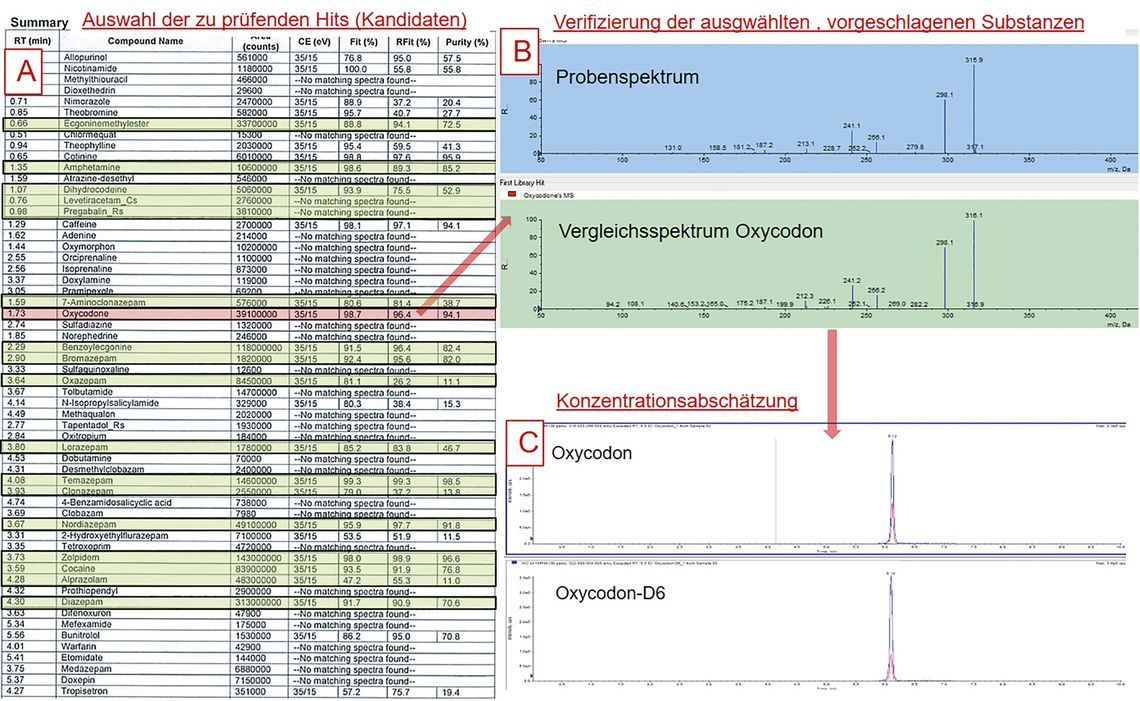
Abb. 2: Ablauf einer toxikologischen Analyse mittels eines Triple-Quadrupol-basierten LC-MS-Systems mit Ionenfalle, bei dem nach Proteinfällung Produktionenspektren aufgenommen werden und eine Hitliste (A) erstellt wird. Dabei werden ausgewählte Hits (grün) mit einer Bibliothek (B) abgeglichen (rot); nach Identifizierung erfolgt eine Konzentrationsabschätzung (C).
Die an struktureller Information reichhaltigsten Analysetechniken stellen neben der GC-MS (gegebenenfalls nach vorheriger Derivatisierung der Analyten) vor allem hochauflösende Massenspektrometer dar, wobei die LC-MS bei der überwiegenden Zahl an Substanzen deutlich kürzere Analysezeiten bei deutlich besserer Nachweisempfindlichkeit aufweist. Sie macht eine Anreicherung im Sinne einer Extraktion in der Vielzahl der Fälle obsolet und spart dadurch deutlich Zeit. GC-MS-Messverfahren bieten allerdings den Vorteil, auch flüchtige Substanzen (wie etwa Methanol, Ethanol oder Propanole) bei Headspace-Injektion identifizieren zu können.
Zur Substanzidentifizierung mittels LC-MS stehen Geräte mit verschiedensten Arten von Ionenfallen sowie unterschiedlicher Massenauflösungen zur Verfügung. Die höchste Spezifität bieten hier hochauflösende Geräte wie Orbitrap- oder Time-of-Flight-Massenspektrometer (TOF). Diese Messgeräte können im entsprechenden Messmodus „General unknown Screenings“ realisieren, wobei die Limitierung des Substanzspektrums neben physikalisch-chemischen Eigenschaften der Substanz hauptsächlich durch den Umfang der Bibliothek besteht. Daneben sind auch zum Beispiel Triple-Quadrupole mit Ionenfalle geeignet, nachweisstarke Screenings zu realisieren. Diese sind im Vergleich zu TOF-/ oder Orbitrap-Screenings allerdings keine „General unknown Screenings“, da bereits im Messmodus eine Limitierung auf bestimmte Substanzen festgelegt wird.
Aber auch die kostengünstigere Kombination aus Flüssigchromatographie-Diodenarray-Detektor (HPLC-DAD) kann in einigen Fällen hilfreich sein. Sie erlaubt meist zumindest eine Zuordnung von Substanzen zu einer strukturellen Substanzklasse, die mittels LC-MS-Screening gegebenenfalls nicht erkannt worden wären, wenn sie nicht in der Bibliothek vorhanden sind (z. B. Designer-Benzodiazepine). Auch hier – wie bei Nutzung von GC-MS – ist eine vorherige Analytanreicherung im Sinne einer Extraktion notwendig, da die Nachweisempfindlichkeit deutlich geringer ist. Wenn man Anreicherungsverfahren wie Flüssig/Flüssig-Extraktion oder Festphasenextraktion nutzt, muss man beachten, dass die kritischen Bedingungen wie pH-Wert und Extraktionsmittel bei Flüssig/Flüssig-Extraktion sowie zusätzlich die Auswahl einer geeigneten Festphase bei Festphasenextraktion (SPE) die Erfassung eines möglichst breiten Substanzspektrums ermöglichen. Prinzipiell gilt, dass die Verfügbarkeit verschiedener Messsysteme und das Wissen über das analytische Potenzial – aber vor allem auch die Grenzen des Nachweises bestimmter Substanzen/Substanzklassen – entscheidend für eine erfolgreiche Bearbeitung von Intoxikationsfällen sind.
