MALDI-TOF-Massenspektrometrie in der molekularbiologischen Diagnostik: Die etwas andere Detektion von SNPs
DOI: https://doi.org/10.47184/td.2023.03.09Die MALDI-TOF-Massenspektrometrie wird im medizinischen Labor häufig für die Identifizierung von Infektionserregern über deren Proteinspektrum eingesetzt. Das Messprinzip eignet sich auch sehr gut für den sensitiven Nachweis von einzelnen Nukleotidveränderungen im Multiplexansatz. Es kann beispielsweise in der Infektions-, Gerinnungs- und Krebsdiagnostik zum Einsatz kommen.
Schlüsselwörter: DNA, cDNA, ccfDNA, Thrombophilie, SARS-CoV-2, personalisierte Krebstherapie
Die molekularbiologische Diagnostik umfasst eine Vielzahl von Untersuchungen in der medizinischen Laborroutine. Das Spektrum reicht vom Nachweis spezifischer RNA- oder DNA-Motive über die Charakterisierung einzelner Gene bis hin zur Analyse des menschlichen Genoms. Üblicherweise wird die Nukleotidsequenz mittels NGS (Next Generation Sequencing) oder früher mittels Sangersequenzierung untersucht. Bei bestimmten Fragestellungen steht aber der Nachweis von einzelnen, definierten Nukleotidveränderungen (Single Nucleotide Polymorphisms, SNPs) im Fokus, die auch zum Nachweis oder zur Differenzierung von Infektionserregern genutzt werden können. Häufig wird eine Kombination von unterschiedlichen SNPs untersucht, die in einem spezifischen klinischen Kontext Relevanz besitzen, sodass Anwendungen, bei denen ein Multiplexansatz möglich ist, besondere Bedeutung zukommt.
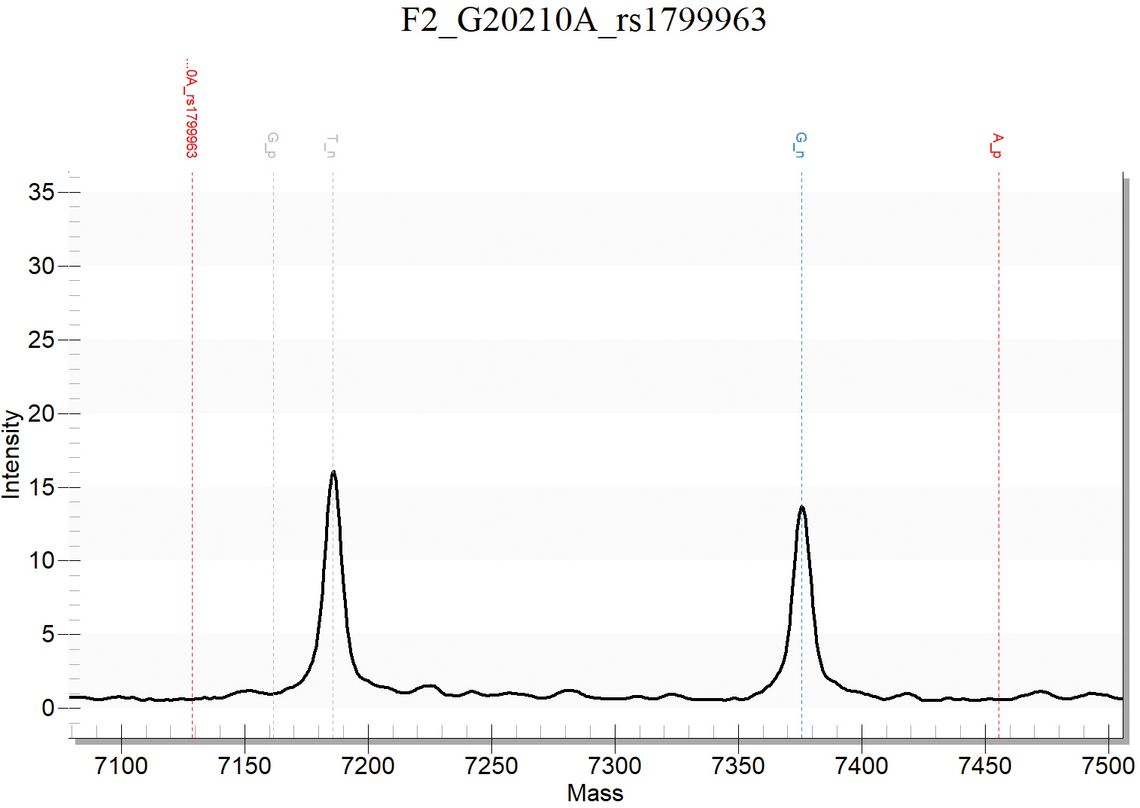
Abb. 1: Prothrombin-G20210A-Assay, Thrombophilie-Panel. Dargestellt ist der Prothrombin-G20210A-Assay in homozygoter Ausprägung mit den drei zugeordneten Massen, die jeweils durch farbige Linien hervorgehoben sind: 7128,6 Da (Extensionsprimer unverlängert), 7375,8 Da (Extensionsprimer verlängert um das Referenznukleotid G) und 7455,7 Da (Extensionsprimer verlängert um das alternative Nukleotid A). Bild: TyperAnalyzer v5.0.2.
Prinzip MALDI-TOF
Eine Technologie, die sowohl den Nachweis einzelner SNPs als auch den Multiplexansatz ermöglicht, ist die massenspektrometrische Analyse von Nukleinsäuren nach dem Prinzip MALDI-TOF (Matrix-Assisted Laser Desorption Ionization – Time Of Flight). Dabei werden in einem dreistufigen Prozess zunächst spezifische Oligonukleotide (Analyten) generiert, die anschließend auf eine Matrix übertragen werden. Mittels kurzer, hochenergetischer Laserpulse kommt es zur Desorption, d. h. der Ablösung der Matrix und der darin eingebetteten Analyten. Durch Abgabe oder Annahme von Protonen werden die Analyten schließlich ionisiert und dann entsprechend ihrer Masse in einem elektrischen Feld beschleunigt und ihre jeweilige Flugzeit gemessen (TOF).
Neben einer stabilen Nachweisgrenze sowohl im Einzel- als auch im Multiplexansatz sind auch Hochdurchsatzanwendungen in einem kosteneffektiven Setting möglich. Die TAT (Turnaround time) von etwa acht Stunden von der DNA-Extraktion über die Amplifikation und der eigentlichen Messung sowie anschließender Auswertung ist relativ kurz. Im Multiplexansatz sind in der Regel ≥ 30 (Keimbahn-)Mutationen oder ≥ 10 somatische Mutationen mit hoher Spezifität parallel detektierbar. Die Kosten für Verbrauchsmaterialen sind dabei nicht von der Anzahl der im Multiplexansatz vereinten Einzeluntersuchungen abhängig, sondern nur von der Anzahl der Mulitplexansätze an sich.
Nachweis von genomischer DNA oder cDNA
Die erreichbare Sensitivität variiert je nach eingesetztem Verfahren mit Detektionslimits von 5 % bis 0,1 % VAF (Variant Allele Frequency). Zunächst wird genomische DNA oder cDNA (complementary DNA = DNA, die aus RNA synthetisiert wurde) mittels PCR amplifiziert. Sobald die initiale PCR abgeschlossen ist, werden überschüssige Nukleotide mittels einer „Shrimp Alkaline Phosphatase (SAP)“-Reaktion dephosphoryliert. Im dritten und letzten Schritt erfolgt eine „Single Base Extension (SBE)“-Reaktion, wodurch die eigentlichen Analyten gebildet werden. Diese bestehen aus dem Oligonukleotid mit bekannter Masse sowie dem durch den SNP bestimmten Nukleotid.
Dazu kommen bei der SBE-Reaktion ddNTPs (Didesoxynukleotide), sog. Terminatoren, anstelle von klassischen dNTPs (Desoxynukleotide) zum Einsatz. Es können auch gezielt die Terminatoren im Überschuss zugegeben werden, die die gesuchte Mutation abbilden. Dies erhöht die Sensitivität von 5 % auf 1 % VAF. Die Analyten werden anschließend entsalzt und von der Mikrotiterplatte durch einen automatischen Nanodispenser auf ein Array übertragen, der die MALDI-Matrix beinhaltet. Nach Abschluss dieses Prozesses wird das Array automatisch in ein MALDI-TOF-Massenspektrometer transferiert, das DNA in einem Messbereich von etwa 4.500 bis 9.000 Da detektiert und zwischen Analyten mit einem Abstand von nur 16 Da unterscheidet. Zum Vergleich: Bei der massenspektrometrischen Analyse von Proteinen zur Differenzierung von Mikroorganismen liegt der relevante Messbereich in der Regel zwischen 2.000 und 20.000 Da.
Nachweis von ccfDNA
Ein hochempfindlicher somatischer Mutationsnachweis kann u. a. für eine Analyse von ccfDNA (circulating cell-free DNA) eingesetzt werden [1]. Das Detektionslimit liegt dann bei 0,1 % VAF. Hierbei kommen ausschließlich Terminatoren zum Nachweis der gesuchten Veränderung zum Einsatz, die zudem mit Biotin markiert sind. Dadurch wird eine Aufreinigung bzw. Anreicherung der generierten Analyten mittels Bindung an Streptavidin ermöglicht und somit die höhere Sensitivität erreicht.
Neben dem Nachweis von Mutationen können mittels MALDI-TOF auch Methylierungen einzelner CpG-Sites oder auch größerer CpG-Islands analysiert werden [2]. Eine basenspezifische Spaltung an Bisulfit-konvertierter DNA ermöglicht eine hochauflösende, quantitative Bestimmung des Methylierungsgrads.
Thrombophilie-Diagnostik
Innerhalb der hämostaseologischen Diagnostik hat die SNP-Analyse von klinisch relevanten Veränderungen, die zu einem erhöhten Risiko für thromboembolische Komplikationen führen, eine ganz zentrale Bedeutung. Wir haben ein Thrombophilie-Panel zusammengestellt, das neben den fest etablierten SNPs (Faktor-V-Leiden, rs6025 und Prothrombin G20210A, rs1799963) auch weitere SNPs berücksichtigt (wie u. a. FSAP G534E, rs7080536; ATIII A384S, rs121909548; FaktorXII C46T; rs1801020 und PAI-1 4G/5G, rs587776796). Dabei werden nicht nur die einzelnen Komponenten unabhängig voneinander bewertet, sondern auch die Kombination. In Abhängigkeit von der klinischen Situation ist somit nicht immer eine Stufendiagnostik sinnvoll, da tatsächlich die Kombinatorik das individuelle Risiko bestimmt. Dieses gilt natürlich nicht nur für rs6025 und rs1799963.
Testung vor Fluorouracil(FU)-haltiger Therapie
In den letzten Jahren hat die Pharmakogenetik massiv an Bedeutung gewonnen. Es ist zum klinischen Standard geworden, dass vor dem Einsatz von 5-Fluorouracil (5-FU) (bzw. Capecitabin und Tegafur) bestimmte SNPs in dem Gen DPYD (rs3918290, rs55886062, rs67376798 und der Haplotyp B3) untersucht werden, um gefährliche Komplikationen aufgrund der Medikamentenmetabolisierung zu verhindern. Gleichermaßen wird mittlerweile auch routinemäßig vor dem Einsatz von Irinotecan das UGT1A1-Gen untersucht. Bei beiden Untersuchungen ist die TAT besonders wichtig, da nach der Feststellung der Therapieindikation der tatsächliche Einsatz der Medikamente von dem Ergebnis der durchgeführten genetischen Untersuchungen abhängt.
SARS-CoV-2 Varianten-Panel
Auch während der SARS-CoV-2-Pandemie konnte die MALDI-TOF-Massenspektrometrie in der Routinediagnostik eingesetzt werden. Im Mittelpunkt stand dabei die SARS-CoV-2-Typisierung: Sie basiert auf charakteristischen Unterschieden an spezifischen Positionen innerhalb des Gens, das das Spike-Protein kodiert. Methodisch bedingt war somit von Anfang an ein Multiplexansatz möglich, der das Ansetzen von einzelnen PCRs pro Position vermied, aber im Verlauf schnell an die sich ändernden Anforderungen angepasst werden konnte. Während zunächst die Differenzierung der Alpha-, Beta- und Gamma-Varianten im Mittelpunkt stand, konnten nach entsprechender Anpassung auch die weiteren neueren Varianten (von Delta bis Omikron) sicher in einem Einzelansatz unterschieden werden. Der Nachweis von Veränderungen an spezifischen Positionen konnte aber nicht nur für die Typisierung genutzt werden, sondern auch zum Nachweis eines Varianten-unabhängigen Immunescapes von SARS-CoV-2 [3] im Kontext einer Resistenzentwicklung.
Abb. 2: SARS-CoV-2-Varianten-Panel v2.1. Dargestellt sind die zehn detektierten Veränderungen im S-Gen einer SARS-CoV-2-Probe sowie der Amplifikationskontrolle „humanes GAPDH“ im Multiplexansatz. Die Kombinatorik aus Referenznukleotiden und Mutationen (inklusive dem Ausfall des E484KQ-Assays) ergibt den SARS-CoV-2-Subtyp BA.1 (Omikron). Bild: TyperAnalyzer v5.0.2.
Assay | Call | Description |
|---|---|---|
GAPDH_Ctrl | A | A.Conservative |
SC2_E484KQ |
| N.No-Alleles |
SC2_H69_V70del_V70F | DEL | A.Conservative |
SC2_K417N | T(N) | A.Conservative |
SC2_L18F | C(WT) | A.Conservative |
SC2_L452QR | T(WT) | A.Conservative |
SC2_N501Y | T(Y) | B.Moderate |
SC2_N856K | A(K) | A.Conservative |
SC2_P681HR | A(H) | A.Conservative |
SC2_T859N | C(WT) | A.Conservative |
SC2_V1176F | G(WT) | A.Conservative |
Individuelle Lösungen
Neben kommerziell erhältlichen Kits können auch individuelle Designs in Form von in-house Panels eingesetzt werden. Bei Forschungsprojekten oder Studien mit spezifischer Fragestellung sind zudem Lösungen möglich, die das ganze Spektrum der SNP- und auch der Methylierungs-Diagnostik umfassen. Service Provider helfen, solche individualisierten Lösungen schnell und zielgerichtet zu etablieren und zur Anwendung zu bringen.
Die massenspektrometrische Analyse von Nukleinsäuren ist eine robuste und schnelle, vielseitige sowie skalierbare und nicht zuletzt kosteneffiziente Technologie, mit der sich viele molekularbiologische Fragestellungen innerhalb eines medizinisch-diagnostischen Labors darstellen lassen.
