Durchflusszytometrie - Viel Potential für die Zukunft
Die Durchflusszytometrie ist vielfältig einsetzbar und erlaubt wertvolle Einblicke in die Physiologie und Pathologie der Zellen, beispielsweise des Immunsystems mit seinen vielfältigen Signalwegen unter Beteiligung zellulärer und subzellulärer Strukturen. Mithilfe einer integrierten Kamera lassen sich neuerdings auch Bilder einzelner Zellen anfertigen, wodurch in Kombination mit Fluoreszenz-Färbungen und KI-gestützter Software neue Erkenntnisse gewonnen und gezieltere Medikamente entwickelt werden können.
Die Durchflusszytometrie gestattet uns eine molekulare Charakterisierung und Quantifizierung von Partikeln, also auch von Zellen, in Suspensionen. Um möglichst vielfältige Aussagen zu erhalten, können bestimmte Zellstrukturen mit Antikörpern, die mit Fluoreszenzfarbstoffen gekoppelt sind, markiert werden. Anschließend passieren die Zellen in einem Hüllstrom vereinzelt eine Durchflusszelle. Dort werden sie gezielt von Lasern angestrahlt. Das von den Zellen gestreute Licht kann aus unterschiedlichen Winkeln von verschiedenen Detektoren gesammelt und sowohl qualitativ als auch quantitativ ausgewertet werden. Aus der Vorwärts(FSC)- und Seitwärts(SSC)-Lichtstreuung lassen sich Größe und Granulation von Zellen beurteilen, während die Lichtstreuung, die durch die Anregung der Antikörpergebundenen Fluoreszenzfarbstoffe hervorgerufen wird, zur Aufklärung molekularer Zusammenhänge beiträgt.
Nach wie vor ist die Durchflusszytometrie dicht an der Forschung angesiedelt, aber die Entwicklung von Assays und Geräten, die in der Routinediagnostik eingesetzt werden können, schreitet parallel voran. Das zeigt sich auch an der zunehmenden Anzahl an CE-IVD-zertifizierten Durchflusszytometern. Vor allem in den Fachgebieten Immunonkologie und Immundefektdiagnostik sowie -therapie sind große Fortschritte zu verzeichnen, die schnell den Weg aus Forschung und Entwicklung in die Anwendung finden. Ein Beispiel ist die Krebstherapie mit CAR-T-Zellen (s. Fachartikel Zelluläre Tumortherapie).
Geräteausstattung funktional
Alle Durchflusszytometer verfügen über ein bis maximal sechs Laser zur Lichtanregung, wobei die Forschungsgeräte naturgemäß über die größte Anzahl
an Lasern verfügen. Um das von den Zellen und Partikeln ausgehende Streulicht aufzufangen, sind in verschiedenen Winkeln zum Laser Detektoren angeordnet, die das Streulicht gezielt auffangen. Dabei kann es sich um Fotodioden, um Photomultipliertubes (PMT) oder neuerdings auch um eine CCD-Kamera (Charge Coupled Device), die Aufnahmen von jeder einzelnen Zelle macht, handeln. Bis zu 28 Fluoreszenzen (s. Tabellarische Übersicht) können erfasst werden. Ohne eine potente Auswertungssoftware wäre die große Datenmenge nicht zu bewältigen und dank der hohen Anzahl an Zellen, die gemessen werden, lassen sich die Ergebnisse der Messungen valide interpretieren. Deshalb hat die Auswertungssoftware hier ein eigenes Kapitel erhalten.
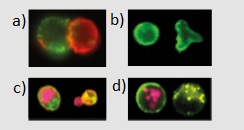
Aufnahmen mit dem Amnis TDI CCD Durchflusszytometer der Fa. Luminex:
a) ZellInteraktion, b) Formveränderung, c) Stammzelle, d) Zelltod und Autophagie.
Messbereich und Nachweisgrenze
Geräte, die in der Routine, beispielsweise zur Messung des Immunstatus, eingesetzt werden, erfüllen mit einem Messbereich über vier oder fünf log-Stufen die Anforderungen voll und ganz, während Forschungs-Durchflusszytometer in der Regel über einen Messbereich verfügen, der bis zu sieben log-Stufen umfasst (vgl. Tabellarische Übersicht). Die Detektionsgrenze geht bei drei Geräten herunter bis auf 25 nm für subzelluläre Strukturen, Organellen, Vesikel etc.. Ein Hersteller gibt an, dass die Messung von Nanopartikeln möglich ist.
Präanalytik und Automatisierung
Ohne eine sorgfältige Präanalytik ist jede Messung ohne Wert. Zum einen haben die Präanalytik und deren Standardisierung große Auswirkungen auf die Ergebnisse; gleichzeitig entlastet sie das Laborpersonal von monotonen, einfachen Arbeiten, wenn beispielsweise große Probenserien vorbereitet werden müssen. Das Pipettieren von Proben und Reagenzien, zu denen auch die Antikörper mit einer begrenzten Haltbarkeit gehören, und die sorgfältige Durchmischung der Proben erfolgt beim überwiegenden Teil der in der Tabelle vorgestellten Geräte außerhalb der Durchflusszytometrie-Einheit durch einen Pipettor oder Liquid Handler. Je nach Gerät werden entweder die Primärproben oder die Reaktionsansätze manuell als Einzelproben über einen Port für Mikrotiterplatten bzw. Reagenzienracks oder ein Probenkarussell in das Durchflusszytometer geladen.
Vollautomatisch arbeiten zwei der in der Tabelle vorgestellten Zytometer. Sie können mit Primärröhrchen bestückt werden; eines der Geräte übernimmt auch das Decapping. Weitere Geräte haben die Probenzufuhr automatisiert, allerdings werden hier die Reaktionsansätze zugeführt, nicht die Primärproben.
Ein anderer Weg zur Unterstützung der Präanalytik und zur Vereinfachung der Lagerung – die dann bei Zimmertemperatur erfolgen kann – sind Röhrchen, die in getrocknetem oder flüssigem Zustand bereits den Antikörper enthalten. Ein Röhrchen entspricht dabei einem Reaktionsansatz.
Zur Automatisierung gehört natürlich auch die Auswertung der Messergebnisse. Wie vielfältig die Darstellungs- und Auswertemethoden sind, ist im Kapitel „Software“ dargestellt.
Anwendungen
Standardanwendungen wie die Quantifizierung von Zellen mithilfe der Durchflusszytometrie müssen hier nicht mehr erläutert werden. Eine klassische Methode ist die Bestimmung der Lymphozyten-Subpopulationen der T- und B-Lymphozyten und NK-Zellen, wie sie beispielsweise zur Immunphänotypisierung erforderlich ist.
Wie oben bereits erwähnt ist die Onkologie eines der Gebiete, in der die Durchflusszytometrie zum Einsatz kommt. So können in einigen Zytometern mittlerweile sogar mazerierte Gewebe, die noch Zelldebris enthalten, zur Messung eingesetzt werden (Primärkulturen, dissoziiertes Tumorgewebe). Als Probenmaterial kommt dann etwa Gewebe aus soliden Tumoren oder von Lymphknoten in Frage. Durch die Mazeration werden Zellen aus dem Zellverbund herausgelöst und sind dadurch für die durchflusszytometrische Analyse zugänglich. Ziel dieser Untersuchungen ist zum Beispiel das Monitoring von Therapien mit sogenannten CAR-T-Zellen (CAR= chimäre Antigenrezeptor-tragende T-Zellen), die in der Onkologie im Rahmen von Zell-basierten Krebstherapien erfolgversprechend eingesetzt werden (s. Fachartikel Zelluläre Tumortherapie).
Eine sehr vielversprechende Erweiterung der Durchflusszytometrie ist die Bildgebung durch die Kombination mit einer Kamera. Dadurch können zelluläre Ereignisse wie NFĸB (Nuclear Factor ĸB)-Translokationen in den Zellkern, Kolokalisationen von Molekülen in Zellen oder zelluläre Formveränderungen sichtbar gemacht werden.
Software
Alle Geräte sind mit spezifischer, in der Regel proprietärer, Auswertungssoftware ausgestattet, mit deren Hilfe die aufgezeichneten Events aus den durchflusszytometrischen Messungen ausgewertet und grafisch aufbereitet werden. Für die Auswertung stehen verschiedene grafische Diagramme wie Streu-/Dichtediagramme oder Histogramme und zahlreiche Statistikoptionen zur Verfügung. Die beiden zusätzlich mit einer Kamera ausgestatteten Durchflusszytometer verfügen über eine mit künstlicher Intelligenz arbeitende Software, die mit selbstlernenden Bildanalyse-Tools Zelltypen noch genauer klassifizieren kann. Zusätzlich zu den oben genannten Diagrammen und Histogrammen erfolgt eine visuelle Auswertung in Form von Einzelbildern. Von jeder Zelle, die die Kamera passiert, wird ein Bild aufgenommen. Durch den zusätzlichen Einsatz von Fluoreszenzfarbstoffen können Signale aus den Zellen aufgenommen werden, die differenziertere Aussagen zum Status einer Zelle zulassen.
Die Software einiger Geräte entspricht den Anforderungen der amerikanischen Food and Drug Administration (FDA) an elektronische Aufzeichnungen und Unterschriften für Medizinproduktehersteller (FDA 21 CFR Part 11-Modus). Ein Durchflusszytometer lässt sich an ein Laborautomationssystem (LAS) anschließen und ist damit besonders für große Probenserien geeignet, wie sie beispielsweise im Rahmen der Medikamentenentwicklung erforderlich sind.
Pflege und Wartung
Pflege und Wartung der Durchflusszytometer sind zwei Punkte, die nicht vernachlässigt werden dürfen. Ganz besonders, wenn man z. B. an mazeriertes Tumorgewebe als Probenmaterial denkt, dass durch die feinen Kapillaren geleitet werden muss. Wir haben in der Tabelle zwischen manuellen und automatisch ablaufenden Reinigungsschritten unterschieden und fragen auch nach der Mean Time Between Failures (MTBF), der Zeit zwischen zwei Geräteausfällen. Die Angaben zur Reinigung sind in der Tabelle ausreichend beantwortet; das gilt auch für die MTBF. Ein Hersteller gibt keine Zahlen an, verweist aber auf eine Funktion der Auswertungssoftware, die Hinweise auf bevorstehende Wartungsschritte gibt (prädiktive Wartung).
Ausblick
Die Kopplung der Durchflusszytometrie mit einer Kamera steht erst am Anfang einer spannenden Entwicklung und verspricht – in Kombination mit einer mit künstlicher Intelligenz ausgestatteten Software – viele neue Erkenntnisse über die Vorgänge in unseren Zellen. Sie kann zu einer immer zielgerichteteren Entwicklung von Medikamenten oder auch zur Prävention von Erkrankungen beitragen. Wenn man zusätzlich noch an die Erforschung extrazellulärer Vesikel denkt, über deren Inhalte unsere Zellen miteinander kommunizieren, sind in Zukunft noch viele spannende Erkenntnisse zu erwarten.
Dr. Gabriele Egert
Jonas Heisterkamp
Prof. Dr. Rudolf Gruber
Mitglieder der Redaktion
Über Trillium Marktübersichten
Der Trillium-Verlag veröffentlicht regelmäßig Marktübersichten über innovative Entwicklungen und Produkte in der Medizin. Dabei fokussieren wir uns auf bewährte und innovative Testverfahren und -systeme aus dem gesamten Spektrum der In-vitro-Diagnostik (Labormedizin, Mikrobiologie, Transfusionsmedizin, Humangenetik, Pathologie und IT). Die Übersichten werden regelmäßig aktualisiert.
Hinweis
Die Sortierung der Anbieter erfolgt in tabellarischen Übersichten und virtuellen Ausstellungsräumen alphabetisch. Die Logos der teilnehmenden Unternehmen werden hingegen randomisiert ausgespielt.
Haftungsausschluss
Sämtliche Marktübersichten (Tabellen, Produktübersichten, virtuelle Industriestände) basieren auf Herstellerangaben und erheben keinen Anspruch auf Vollständigkeit und Richtigkeit; die Teilnahme ist kostenpflichtig. Wir weisen Sie im i. S. d. Bayerischen Pressegesetzes Artikel 9 ausdrücklich darauf hin, dass die Inhalte der virtuellen Industriestände werbend sind.