Zelluläre Funktionstests in der Immunologie: Von A(llergie) bis Z(ytotoxizität)
DOI: https://doi.org/10.47184/td.2022.01.04Antikörpernachweise sind seit Langem fester Bestandteil der labormedizinischen Diagnostik. Mittlerweile haben auch viele Untersuchungen der zellulären Elemente des Immunsystems Einzug in die Routinediagnostik gehalten. Neben der Reaktivität von T-Zellen können auch die zytotoxische Funktion von natürlichen Killerzellen, die Phagozytenfunktion und die Basophilendegranulation beurteilt werden. All diese Tests stellen hohe Anforderungen an die (Prä-)Analytik und machen das Einhalten von Qualitätsstandards dringend erforderlich.
Schlüsselwörter: Lymphozytentransformationstest, ELISpot, Durchflusszytometrie, Migratest, NBT-Test, BDT, BAT
Für die Erhaltung der Integrität des Organismus spielt das Immunsystem mit seinen angeborenen und erworbenen Mechanismen eine zentrale Rolle. Zur Erfassung von spezifischen Immunantworten sind im medizinischen Labor vor allem Antikörpernachweise fester Bestandteil der Diagnostik. Immunglobuline können typischerweise stabil im Serum nachgewiesen und mit gut etablierten Immunoassays routinetauglich erfasst werden. Bei vielen Infektionen, aber auch bei Autoimmunerkrankungen, Allergien oder Immundefekten ist die Bestimmung von spezifischen Antikörpern oder von Immunglobulinklassen ein wesentliches Element des diagnostischen Prozesses.
Die Untersuchung der zellulären Elemente des Immunsystems birgt für die medizinische Routine viele Herausforderungen. Meist müssen die Untersuchungen an frischem Blut durchgeführt werden, was hohe Anforderungen an Präanalytik und an die Analytik selbst stellt. Unterscheiden lassen sich Untersuchungen, bei denen Zellpopulationen quantifiziert und Aussagen über ihren Differenzierungs- und Aktivierungszustand getroffen werden können, und funktionelle Tests, die beispielsweise zelluläre Immunantworten analysieren. Die Quantifizierung und Charakterisierung von Zellpopulationen erfolgt in der Regel durch eine Immunphänotypisierung mittels Durchflusszytometrie [1, 2].
Funktionelle Untersuchungen sind so aufgebaut, dass die Zellen im Vollblut oder nach Isolation mit geeigneten Stimulatoren inkubiert und so aktiviert werden. Die Folgen dieser zellulären Aktivierung lassen sich dann nachweisen, und zwar entweder als totale Antwort der eingesetzten Zellprobe (engl. bulk assay) oder auf dem Niveau von Einzelzellen. Beispiele für Bulk Assays sind beispielsweise die Freisetzung von Zytokinen oder der Nachweis einer Zellproliferation. Solche Testverfahren sind technisch wenig komplex – vorausgesetzt das Labor verfügt über die Logistik für die Einhaltung der Präanalytik sowie die notwendige Ausrüstung und Erfahrung im Umgang mit zellulären Proben. Dies limitiert die Etablierung solcher Methoden auf wenige spezialisierte Labore.
Untersuchungen auf Einzelzellniveau können Phänotypisierung und funktionelle Testung kombinieren und erlauben daher sehr viel spezifischere Aussagen über die Antwort bestimmter Zellpopulationen. Eine solche Analysentiefe kann unter bestimmten Umständen notwendig sein, um protektive Immunantworten zu detektieren, wie in verschiedenen Studien gezeigt werden konnte [3]. Aktuell sind solche Verfahren wegen ihrer Komplexität eher der Forschung vorbehalten. Mit der stürmischen Verbreitung von Vielfarb-Durchflusszytometern werden sie aber auch in die Routinediagnostik Einzug halten.
Wir konzentrieren uns im Folgenden auf funktionelle Untersuchungen, die in der Routinediagnostik verwendet werden.
Reaktivität von T-Zellen
Stimulation durch Mitogene
Seit Langem etabliert und immer noch weit verbreitet sind Tests, die auf der Messung eingebauter radioaktiv markierter Substanzen basieren. Ein prominentes Beispiel ist der Lymphozytentransformationstest (LTT), ein basaler Test für die Untersuchung der Stimulierbarkeit von Zellen zur Proliferation. Die Zellen werden dazu über eine Dichtegradientenzentrifugation getrennt und typischerweise für drei Tage mit Mitogenen stimuliert. Mitogene sind polyklonale Aktivatoren, die bevorzugt T-Zellen (z. B. Concanavalin A oder Phytohämagglutinin) oder B- und T-Zellen (Pokeweed-Mitogen) aktivieren. Nach der Inkubation werden die Zellen einfach gezählt oder aber sich teilende Zellen markiert. Klassischerweise erfolgt die Markierung über den Einbau von 3H-markiertem Thymidin in die DNA. Aufgrund der hohen regulatorischen Anforderungen im Umgang mit Radioaktivität und der stetig steigenden Entsorgungskosten sind radioaktiv basierte Funktionstests aus heutiger Sicht für viele Labore nicht mehr sinnvoll und werden durch andere Verfahren abgelöst.
Mittlerweile sehr gut etablierte Alternativen sind beispielsweise die Verwendung nicht-radioaktiver Nukleotidanaloga wie Bromodexyuridin, Ethynyldeoxyuridin, Farbstoffe wie VPD450 (Violet Proliferation Dye 450) und CFSE (Carboxyfluorescein-Succinimidyl-Ester) oder der Nachweis einer verstärkten Stoffwechselaktivität (zum Beispiel mittels 3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazoliumbromid (MTT)). Besonders vorteilhaft gegenüber den radioaktiven Methoden sind der Wegfall der strengen Regularien (Personalschulung, entkoppelte Laborräume, radioaktiver Müll), der Ansatz als einfacher durchflusszytometrischer Funktionsassay, und die Auswertung von gut sichtbaren Zellwolken oder Peaks sich teilender Zellen. Bei Verwendung interkalierender Farbstoffe kommt allerdings deren genotoxisches Potenzial hinzu.
Eingesetzt werden solche Mitogen-LTTs vorwiegend in der Diagnostik primärer Immundefekte, um eine generelle Orientierung über die Stimulierbarkeit der Lymphozyten zu erhalten. Sie sind daher auch Bestandteil der entsprechenden Klassifikationskriterien.
Antigen-spezifische T-Zell-Antwort
Grundsätzlich eignet sich der LTT aber auch zum Nachweis einer Antigen-spezifischen T-Zell-Antwort im Bereich der Typ-IV-Sensibilisierung. Der Nachweis solcher Antworten ist klinisch relevant bei der Abklärung von nicht-IgE-vermittelten allergischen Reaktionen. Diese sind beispielsweise die weit verbreiteten Allergien gegen Nickel und andere Metalle, aber auch die Sensibilisierungen gegenüber Acrylaten, die unter anderem in Pflastern und Kunststoffen vorkommen.
Erreger-spezifische T-Zell-Antwort
Ein weiteres Einsatzgebiet der Untersuchung der T-Zell-Reaktivität ist der Nachweis von erregerspezifischen Immunantworten. Prominentestes Beispiel ist hier der Nachweis einer zellulären Immunität nach Kontakt mit Mycobacterium tuberculosis mittels Enzyme Linked Immuno Spot Assay (ELISpot), dessen Readout allerdings nicht auf der Proliferation der spezifischen T-Zellen, sondern auf dem Nachweis einer Interferon(IFN)-gamma-Freisetzung beruht. Dabei werden die isolierten Zellen in einer beschichteten Mikrotiterplatte inkubiert und die Anzahl der reagierenden Zellen wird über den Nachweis sezernierter Produkte (Immunglobulin, Zytokine) als Spot in der Zellumgebung nachgewiesen.
Aktuell zeichnet sich ab, dass dies auch bei Cytomegalovirus (CMV) und SARS-CoV-2 [4] eine gewisse Bedeutung erlangen könnte. Bei ausreichend robusten Tests und wenn die exakte Differenzierung der aktivierten Zellen nicht erforderlich ist, ist der ELISpot eine sinnvolle, routinetaugliche und gut etablierte Methode (Abb. 1).
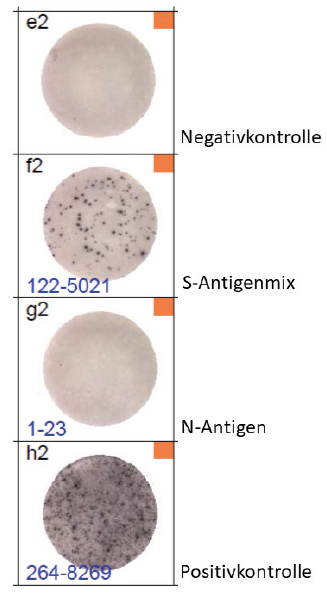
Abb. 1: ELISpot nach 16-stündiger Stimulation eines gegen SARS-CoV-2 geimpften Probanden.
Freigesetzte Zytokine wie IFN-gamma und Interleukin(IL)-2 können natürlich auch per ELISA im Überstand gemessen werden; dann fallen aber einzelzellbezogene Informationen weg.
Die Bedeutung des LTTs für die Diagnostik ist ein kontrovers diskutiertes Thema. Als Kritikpunkte werden oft und berechtigt die mangelnde Standardisierung der Tests zwischen den verschiedenen Laboren und Methoden sowie die aufgrund fehlender klinischer Studien unsichere klinische Aussagekraft angeführt. Dem kann entgegengehalten werden, dass der In-vitro-Nachweis von Immunantworten objektiv, robust und reproduzierbar ist – ganz im Gegensatz zu den ansonsten verwendeten Hauttests (Epi- oder Intrakutantest), die vielen äußeren Einflüssen unterliegen.
Durchflusszytometrische Verfahren
Neben der Proliferation sind mittlerweile auch andere Möglichkeiten zum Nachweis einer zellulären Aktivierung durch Mitogene oder Antigene etabliert worden:
- die Signaltransduktion (Signal Transducer And Activator Of Transcription 5(STAT-5)-Phosphorylierung [5]),
- die Expression aktivierungsabhängiger Oberflächenmoleküle (CD69, CD40L oder CD137) oder
- eine Zytokinfreisetzung (z. B. IFN-gamma).
Der Nachweis dieser Veränderungen erfolgt in aller Regel durch die Durchflusszytometrie. Hier können, wie bereits oben erwähnt, Oberflächenmarker zur Identifizierung von Zellpopulationen verwendet werden, sodass eine sehr viel differenziertere Analyse möglich ist. Ein weiterer Vorteil dieser alternativen Methoden liegt darin, dass oft nur eine kurzzeitige Stimulation erforderlich ist, z. B. pSTAT-5 in 24 Stunden. Die Stimulation des LTT mit Mitogenen erfordert eine Inkubationszeit von drei, mit Antigenen sogar von fünf Tagen. Diese lange Inkubationszeit führt zu der sehr hohen Sensitivität des LTT, da auch sehr geringe Frequenzen von Antigen-spezifischen T-Zellen ausreichend expandieren und zu einem messbaren Signal führen können.
Die Lymphozytenmischkultur ist im Grunde eine Sonderform des LTT und wird zur Bestimmung der Verträglichkeit zwischen Spender- und Empfängerzellen eingesetzt. Hier ist eine Inkubationszeit von einer Woche gebräuchlich.
Zytotoxizität
In der Immunabwehr gegen Tumoren nehmen natürliche Killerzellen (NK-Zellen) eine zentrale Rolle ein. Die zytotoxische Funktion von NK-Zellen kann durch einen Bioassay unter Verwendung von echten Tumorzellen (Bioptat, Operationsmaterial, Liquid Biopsy) oder von NK-Zelllinien (K562) überprüft werden. Die Zielzellen können radioaktiv- (Chrom-51-Freisetzung) oder fluoreszenzmarkiert eingesetzt werden, um ihre Lyse direkt nachzuweisen. Gebräuchlicher ist aber im Labor der zytometrische Nachweis von CD107a auf den NK-Zellen. Dieser Marker ist eng mit der Freisetzung der zytotoxischen Granula verbunden. Das Untersuchungsverfahren lässt sich auch auf zytotoxische T-Zellen übertragen. Eine gesicherte Indikation für derartige Tests ist der Nachweis eines Degranulationsdefektes bei der hämophagozytischen Lymphohistiozytose (HLH). Kontrovers diskutiert wird eine Modifikation des Tests, bei der während der Zellkultur verschiedene Compounds hinzugefügt werden, um eine Verstärkung der Zytotoxizität zu erreichen und Kandidaten für eine gezielte Therapie zu identifizieren. Hier ist die Standardisierung noch nicht weit fortgeschritten.
Phagozytenfunktion
Für die angeborene Immunität, aber auch in der Effektorphase der erworbenen Immunität sind Phagozyten unentbehrlich. Sie werden über Chemotaxis angelockt, wandern zur Stelle der Immunreaktion, adhärieren an Zielmolekülen, phagozytieren Material und töten mit dem oxidativen Burst Erreger ab. All diese Schritte können im Labor untersucht werden. Chemotaxis und Migration wurden ursprünglich in der Boyden-Kammer analysiert; heute werden im Speziallabor mikrofluidische Systeme oder ein durchflusszytometrischer Test zur Untersuchung der Migration eingesetzt. Letzterer trägt zudem das CE-Label und kann somit einfach im Routinelabor verwendet werden (Abb. 2) [6].
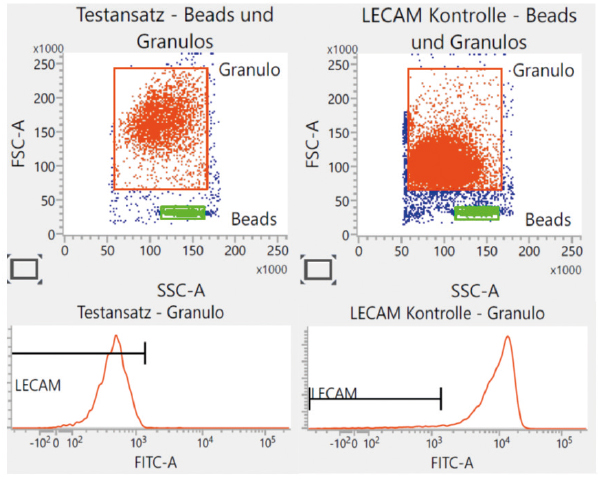
Abb. 2: Untersuchung der Migration im Durchflusszytometer. Granulozyten wandern durch eine poröse Membran auf N-Formylmethionyl-leucyl-Phenylalanin (fMLP) zu und verlieren dabei endotheliale Leukocyten-Adhäsionsmoleküle (LECAM).
FSC = forward scatter, SSC = side scatter, FITC = Fluorescein-Isothiocyanat.
Phagozytose und oxidativer Burst (Aktivierung der Nicotinsäureamid-Adenin-Dinukleotid-Phosphat(NADPH)-Oxidase) werden meist gemeinsam untersucht: Fluoreszenzmarkierte Erreger werden phagozytiert und die intrazelluläre Abtötung wird über ein fluorogenes Substrat gemessen [7]. Auch dieses Verfahren steht als In-vitro-Diagnostikum zur Verfügung. Zudem gibt es für die Untersuchung des oxidativen Bursts noch den Nitro-Blue-Tetrazolium (NBT)-Test [8]. Da hier nur wenige Zellen benötigt werden, wird der Test vereinzelt noch in pädiatrischen Laboren durchgeführt. Wegen der besseren Standardisierung geht der Trend aber eindeutig in Richtung Durchflusszytometrie. Indiziert sind diese Untersuchungen fast ausschließlich bei der Diagnostik angeborener Immundefekte.
Basophilendegranulation
Bei der IgE-vermittelten Allergie lösen Allergene über an Fcε-gebundene IgE-Moleküle eine Mastzelldegranulation aus. Diese kann auch an Basophilen aus dem peripheren Blut untersucht werden, wobei insbesondere der funktionelle Aspekt durch die Quervernetzung der Fcε-Rezeptoren zusätzliche Informationen liefert. Die Aktivierung der Basophilen führt dabei zur Freisetzung zahlreicher Mediatoren, die im Überstand gemessen werden können, und zur Veränderung von Zelloberflächenmolekülen, die im Durchflusszytometer untersucht werden. Dementsprechend gibt es diese Tests in zwei verschiedenen Ausführungen, einmal mit nachfolgendem ELISA (Basophilen-Degranulations-Test; BDT), oder im Durchflusszytometer (Basophilen-Aktivierungstest; BAT). Hier wird entweder die Heraufregulation von CD203c [9] oder CD63 [10] gemessen.
Klinische Indikationen für den Einsatz dieser Tests sind:
die In-vitro-Diagnostik einer IgE-vermittelten Allergie bei nicht-nachweisbarem freien IgE
Bedingt durch die geringe Konzentration und kurze biologische Halbwertszeit des IgE lassen sich möglicherweise trotz einer klinisch vermuteten Typ-I-Allergie keine spezifischen IgE-Antikörper gegen das fragliche Allergen nachweisen. In solchen Fällen ist es sinnvoll, eine zelluläre Testung mittels BAT/BDT durchzuführen, da auf der Oberfläche von Mastzellen und Basophilen gebundenes IgE eine deutlich höhere Stabilität aufweist und man noch Typ-I-Sensibilisierungen nachweisen kann.
ein unbekanntes oder seltenes Allergen
Unter Umständen ist für ein vermutetes Allergen kein Test zum Nachweis von spezifischem IgE erhältlich. Auch hier kann eine zelluläre Allergiediagnostik helfen, in vitro eine Sensibilisierung nachzuweisen. Relevant ist dies insbesondere bei Medikamenten.
Pseudoallergien
Pseudallergien werden durch eine nicht-IgE-vermittelte Aktivierung von Mastzellen verursacht. Eine Pseudoallergie lässt sich also nicht durch eine Bestimmung von IgE-Antikörpern nachweisen, sodass sich auch hier ein Einsatzgebiet für den BAT/BDT ergibt (Abb. 3).
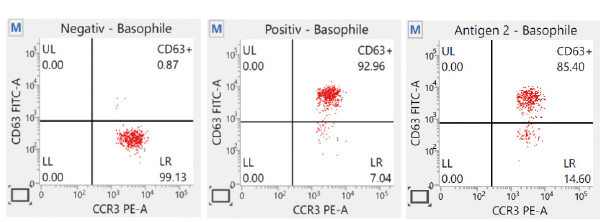
Abb. 3: Nachweis einer Allergie auf Polysorbat 80 (1:100) mittels Flow-BAT gegenüber Negativ- und Positivkontrolle. FITC = Fluorescein Isothiocyanat, CCR3 = C-C Chemokin Rezeptor Typ 3, PE-A = Phycoerythrin A, UL = oberer linker Quadrant, LL = unterer linker Quadrant, LR = unterer rechter Quadrant.
Einsatz im Routinelabor
Wie beschrieben gibt es eine Vielzahl unterschiedlicher Funktionstests, die in verschiedenen Anwendungsgebieten eingesetzt werden können. Sie sind in der diagnostischen Kaskade ein sinnvolles Hilfsmittel, um z. B. primäre Immundefekte einzugrenzen, latente Infektionen oder Impfantworten nachzuweisen (ELISpot, STAT5-Phoshorylierung) oder IgE-vermittelte Allergien besonders sensitiv nachzuweisen.
Bei langwierigen Tests mit Stimulationszeiten über mehrere Tage ist es sinnvoll, nach neuen Markern zu suchen, die als alternative Schnelltests verwendet werden können und der behandelnden Person damit schneller therapeutische Optionen eröffnen. Beispielhaft ist hier der Nachweis der STAT5-Phosphorylierung (max. 24 h) als schnelle Alternative zu den länger andauernden Proliferationstests (mind. drei Tage) zu nennen.
Wenn die Tests im Routinelabor durchgeführt werden, müssen Qualitätsstandards eingehalten werden. Die Tests sollen nur bei gesicherter Indikation angewendet werden und müssen im Labor verifiziert oder bei Modifikationen validiert werden. Die Unterlagen dazu müssen insbesondere auch mit Blick auf die neue IVD-R dokumentiert sein. Als interne Qualitätskontrolle wird typischerweise – sofern das Testformat keine eigene Kontrollstrategie hat – das Blut einer altersgematchten gesunden Kontrolle mitgeführt. Ringversuche oder Laborvergleich sichern die externe Qualitätskontrolle. Sollte beides nicht möglich sein, ist nach einer anderen Strategie zu suchen, um den korrekten Testverlauf sowohl für positive als auch negative Ergebnisse zu sichern.
Für die Interpretation muss berücksichtigt werden, dass die Referenzintervalle häufig eine sehr große Spannweite aufweisen.
Allerdings setzt jeder zelluläre Funktionstest immer eine gewisse Kenntnis der immunologischen Signalkaskade voraus. So ist es wenig sinnvoll, bei einer IgE-vermittelten Immunantwort den Nachweis von IgG zu erbringen. Beim Nachweis erregerspezifischer T-Zellen müssen die geeigneten Antigene in hoher Qualität zur Verfügung stehen. Im Gegensatz zur Serologie sind die für eine Immunität notwendigen Konzentrationen positiver T-Zellen, die sich ja auch während des Assays teilen, nur in Einzelfällen bekannt.
Zusammengefasst sind moderne zelluläre Funktionstests ein wichtiger Bestandteil der diagnostischen Kaskade und bringen, sinnvoll eingesetzt, schnell und gezielt neue Erkenntnisse über zelluläre Defekte, fehlende Impfantworten, latente Infektionen oder mögliche Allergien.
Tab. 1: Überblick über zelluläre Funktionstests in der Routinediagnostik.
| Test | Testprinzip | Anwendung |
|---|---|---|
| Reaktivität von T-Zellen | ||
| Lymphozytentransformationstest | Stimulation der T-Zellen mit Mitogenen oder Antigenen, anschließende Markierung mit radioaktiven Nukleotid-Analoga; alternativ: Markierung mit Farbstoffen und durchflusszytometrische Auswertung | Diagnostik primärer Immundefekte (Mitogen) und nicht-IgE-vermittelter allergischer Reaktionen (Antigen) |
| Enzyme Linked Immuno Spot Assay (ELISpot) | Untersuchung einer erregerspezifischen T-Zell-Antwort durch den Nachweis einer Interferon(IFN)-gamma-Freisetzung | Nachweis von erregerspezifischen Immunantworten (z. B. M. tuberculosis) |
| Zelluläre Allergiediagnostik | ||
| Basophilenaktivierungstest | Stimulation von Basophilen mit Allergenen, danach Messung der Freisetzung von Histamin oder Leukotrienen (ELISA) oder einer Stimulation der Zellen über CD63 oder CD203c (Zytometrie) | Funktioneller Nachweis IgE-vermittelter Allergien |
| Zytotoxizität (NK- und T-Zellen) | ||
| Bioassay | Verwendung von echten Tumorzellen oder von NK-Zelllinien, Nachweis der Lyse von radioaktiv- oder fluoreszenzmarkierten Zielzellen | Nachweis eines Degranulationsdefektes bei der hämophagozytischen Lymphohistiozytose |
| Nachweis von CD107a | Durchflusszytometrie | |
| Phagozytenfunktion | ||
| Untersuchung von Chemotaxis/Migration | Mikrofluidik oder Durchflusszytometrie | Diagnostik angeborener Immundefekte |
| Untersuchung von Phagozytose/oxidativem Burst | Phagozytose von fluoreszenzmarkierten Erregern mit Messung der intrazellulären Abtötung über ein fluorogenes Substrat | |
| Untersuchung des oxidativen Burst | Nitro-Blue-Tetrazolium (NBT)-Test | |


