
Besuchen Sie unsere Website und lernen Sie unsere Lösungen für Ihr Labor kennen.
Die europäische Verordnung über In-vitro-Diagnostika (IVDR) (EU) 2017/746 trat am 26. Mai 2017 in Kraft und wird die europäische Richtlinie über In-vitro-Diagnostika (IVDD) 98/79/EG ersetzen. Ein globales funktionsübergreifendes Team bei BD Biosciences hat daran gearbeitet, die neue Verordnung nahtlos und konform umzusetzen.
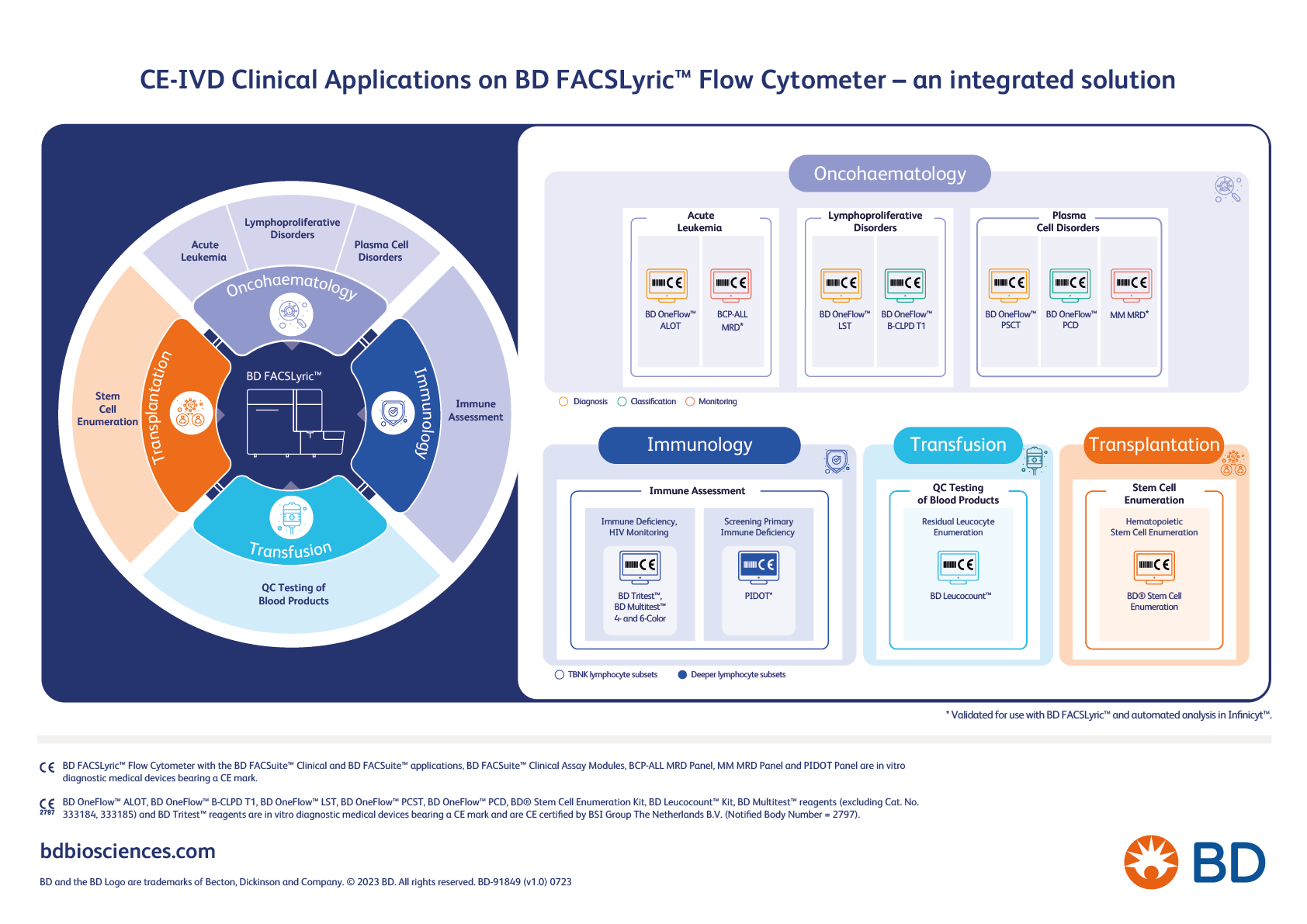
Das für die IVDR-Konformität vorgesehene Reagenzienportfolio von BD Biosciences umfasst In-vitro-Diagnostik Lösungen für*
- Immunphänotypisierung von hämatologischen Erkrankungen mittels Durchflusszytometrie
- Überwachung von HIV-infizierten Personen
- Charakterisierung und Überwachung von Immunschwäche und Autoimmunkrankheiten
- Zellauszählung von Blutprodukten für Transfusions- und Stammzellentransplantationsverfahren
Das IVDR-Portfolio von BD Biosciences wird auch Durchflusszytometer und Automatisierungslösungen umfassen.
*Nach dem IVDR-Anwendungsdatum werden die auf dieser Seite angegebenen Produkte als IVDR-konforme Produkte und/oder als IVDD-konforme Produkte zur Verfügung gestellt.
Besuchen Sie auch unsere englischsprachige Infoseite zum Thema IVDR.

Tullastr. 8-12
69126 Heidelberg
BD Life Sciences – Biosciences




